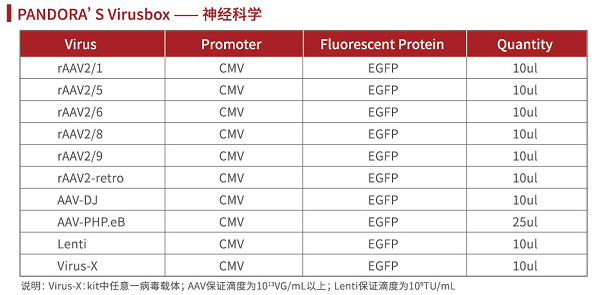
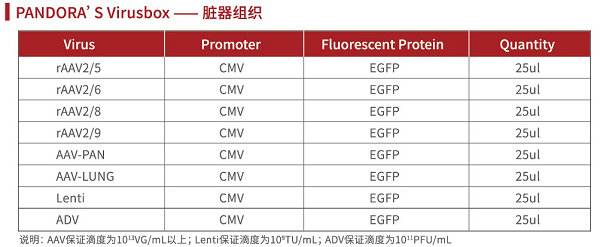
腺相关病毒(adeno-associated virus, AAV)是微小病毒科(parvoviridae)家族的成员之一,是一类无法自主复制、无被膜的二十面体微小病毒,其直径约20-26nm,含有4.7kb左右的线状单链DNA作为基因组。研究中采用的重组腺相关病毒载体(recombination adeno-associated virus, rAAV)是在非致病的野生型AAV基础上改造而成的基因载体,由于其种类多样、免疫原性极低、安全性高、宿主细胞范围广(对分裂细胞和非分裂细胞均具有感染能力)、扩散能力强、体内表达基因时间长等,rAAV被视为最有前途的基因研究和基因治疗载体之一。
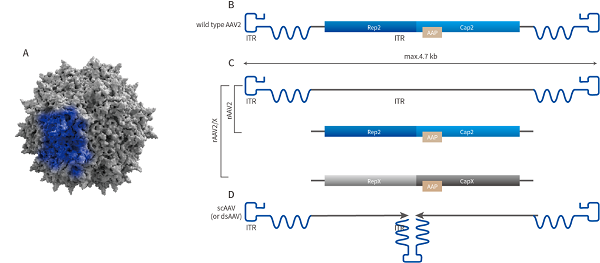
AAV基因组结构
rAAV包装纯化及滴度检测
AAV包装过程中,包装质粒负责编码目的基因以及两个末端反向重复序列(ITR,对于病毒的复制和包装具有决定性作用),辅助质粒包含AAV包装所需的cap(编码病毒衣壳蛋白)和rep(参与病毒的复制)基因,以及腺病毒Helper质粒。三种质粒共同转染293T细胞后,AAV病毒开始复制和包装。腺相关病毒的生产和质控采取了国际学术界公认的标准流程,采用三质粒系统在293T细胞中进行包装。所获得的病毒颗粒经过超速离心纯化,并通过qPCR对病毒基因拷贝进行滴定。另外,我们也可以根据使用者要求,提供蛋白染色检测衣壳蛋白的完整性以及内毒素含量等。一般情况下rAAV的滴度在1012~1013 VG/ml,完全可以满足各类整体实验的使用要求。
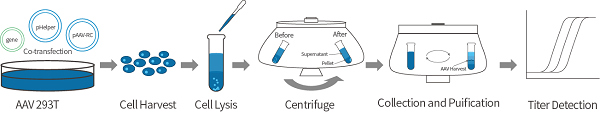
AAV包装流程图
滴度检测方法:定量PCR检测病毒基因组中外源DNA拷贝数。
滴度检测原理:腺相关病毒的基因组为单链DNA,外源DNA拷贝数代表病毒基因组拷贝数。
rAAV侵染细胞过程
纯化后的AAV病毒载体可以用于侵染细胞,侵染细胞时,AAV与细胞表面特异性受体结合,激活胞内信号通路,进而触发AAV通过受体介导的内吞作用进入细胞,在核内体、高尔基体等细胞器的协助下进入细胞核,随后病毒裂解,其单链DNA需复制成为双链DNA后表达目的基因。
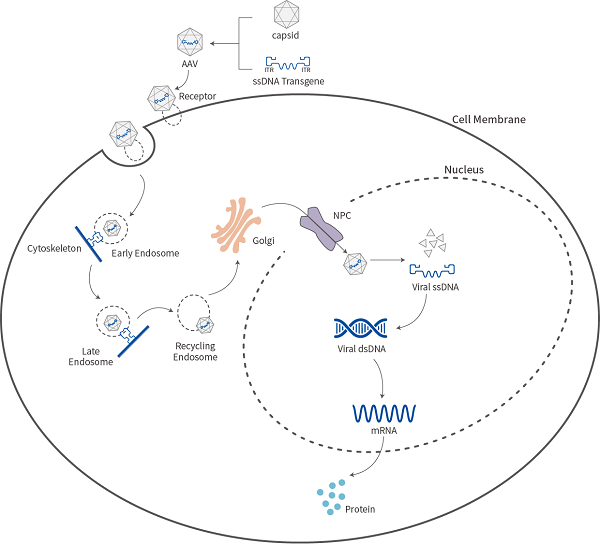
rAAV作用机制
rAAV载体优势
1、安全性高、免疫原性低:AAV是一种复制缺陷型DNA病毒,无自主复制能力,野生型AAV依赖rep基因进行低频定点整合,rAAV不整合。目前尚无由AAV引起的人类及哺乳动物疾病报道,也是FDA批准上市的基因治疗药物中最安全的病毒载体之一。
2、宿主细胞范围广:AAV具有广泛的宿主范围,对分裂细胞和非分裂细胞均具有感染能力。
3、扩散能力强:AAV直径约20-26nm,体积小,滴度高,具有良好的扩散能力,其中AAV-PHP.eB和AAV9具有跨血脑屏障的能力,在神经科学领域应用广泛。
4、体内表达基因时间长:AAV具有保持长期基因转录表达能力,体内表达一般3周可以达到高峰,随后持续高表达,作用时间>5个月。
5、种类多样:AAV血清型众多,此外,根据不同的实验设计,我们还在不断的突变,筛选新的血清型(AAV1-13,AAV2/1, 2/2, 2/5, 2/6, 2/8, 2/9, DJ; retro, PHP.eB…)。
不同病毒的生物学特性比较
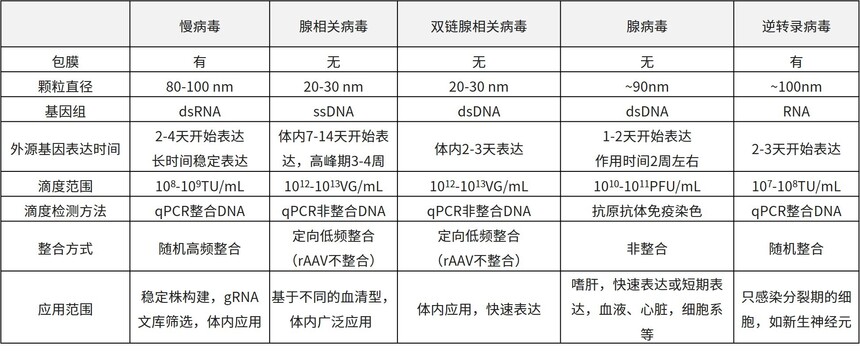
基于上述特点,AAV被视为是一种高效和安全的体外及体内基因转导工具。尤其在整体水平研究中,与其他常用病毒工具载体相比,AAV具有感染过程温和长效的表达能力,是基因操作的利器。
rAAV血清型选择
目前已注册的AAV种类总数已超过196种,灵长类动物体内有13种不同血清型的AAV(即AAV1-AAV13),其中AAV2、AAV3、AAV9源自人类本身,值得注意的是,AAV2是最早被克隆的病毒,也是迄今研究最为彻底、应用最为广泛的病毒载体。随着研究的不断深入,研究人员发现不同血清型的AAV之间可以杂交,而杂交后的AAV会兼有杂合双方的特点,因此,AAV亚型顺势诞生。
现在研究中常用的rAAV就是利用AAV2型基因组与不同的衣壳蛋白结合产生的混合体病毒载体,一般标记为rAAV2/N (N为不同的衣壳血清型)。重组的病毒具有AAV2型的稳定表达和基因整合能力,同时获得了不同血清型的组织感染嗜亲性(不同血清型衣壳表面的特定结构位点决定了各自受体的特异性),表现出一定的器官靶向特异性。
不同血清型AAV的组织嗜亲性
| 血清型 | 组织亲和性 |
| rAAV2/1 | 神经系统(高滴度顺向跨突触),肌肉,骨骼肌,心肌,平滑肌 |
| rAAV2/2 | 视网膜、神经系统,肌肉,肝脏,血管平滑肌 |
| rAAV2/3 | 肌肉,肝脏,肺,眼 |
| rAAV2/4 | 神经系统,肌肉,眼,脑 |
| rAAV2/5 | 神经系统,肺,视网膜,肝脏,滑膜关节 |
| rAAV2/6 | 神经系统,肺,肌肉,心脏 |
| rAAV2/7 | 肌肉,肝脏 |
| rAAV2/8 | 神经系统,肝脏,肌肉,脂肪组织,胰腺,视网膜, |
| rAAV2/9 | 神经系统,心肌,肺,视网膜,皮肤 |
| rAAV2-retro | 神经系统(逆向非跨突触) |
| AAV-PHP.eB | 跨血脑屏障(静脉注射) |
| AAV-PHP.S | 全外周神经(尾静脉注射) |
| AAV-PAN | 胰腺(腹腔注射) |
| AAV-LUNG | 肺(尾静脉注射) |
| AAV-DJ | 视网膜,肺,肾脏,体外感染细胞 |
| AAV-7m8 | 视网膜 |
| AAV-ShH10Y | 视网膜Muller细胞 |
| AAV-Rh10 | 肝脏,血液,心脏,体外感染细胞 |
| AAV-Anc80L65 | 内耳、视网膜、骨骼肌、肝脏 |
| AAV-SCH9 | SVZ区神经干细胞 |
小建议:如您不确定选择哪种血清型,可尝试使用Pandora’s Virus (AAV多种血清型)进行预实验,通过比较不同血清型对目标组织的感染效果,摸索最佳实验条件(注射方法、注射位点、病毒用量等),以便得到更理想的实验结果。
Pandora’s Virus 详情: